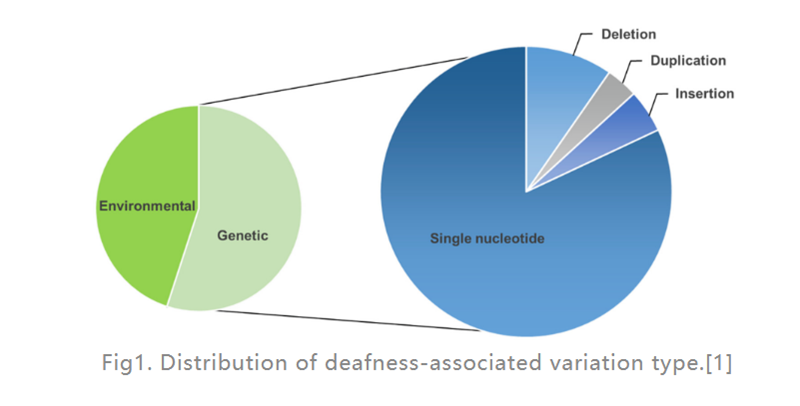
کم شنوایی (HL) شایع ترین بیماری ناتوانی حسی در انسان است.در کشورهای توسعه یافته، حدود 80 درصد موارد ناشنوایی پیش زبانی در کودکان ناشی از عوامل ژنتیکی است.شایع ترین آنها نقص های تک ژنی هستند (همانطور که در شکل 1 نشان داده شده است)، 124 جهش ژنی با کم شنوایی غیر سندرومی در انسان مرتبط هستند، بقیه توسط عوامل محیطی ایجاد می شوند.کاشت حلزون (دستگاه الکترونیکی که در گوش داخلی قرار می گیرد و تحریک الکتریکی را مستقیماً به عصب شنوایی ارائه می کند) تا حد زیادی مؤثرترین گزینه برای درمان HL شدید است، در حالی که یک سمعک (یک دستگاه الکترونیکی خارجی که امواج صوتی را تبدیل و تقویت می کند) می تواند به بیماران مبتلا به HL متوسط کمک کند.با این حال، در حال حاضر هیچ دارویی برای درمان HL ارثی (GHL) در دسترس نیست.در سال های اخیر، ژن درمانی به عنوان یک رویکرد امیدوارکننده برای درمان اختلال عملکرد گوش داخلی مورد توجه فزاینده ای قرار گرفته است.
عکس. 1.توزیع نوع تنوع مرتبط با ناشنوایی.[1]
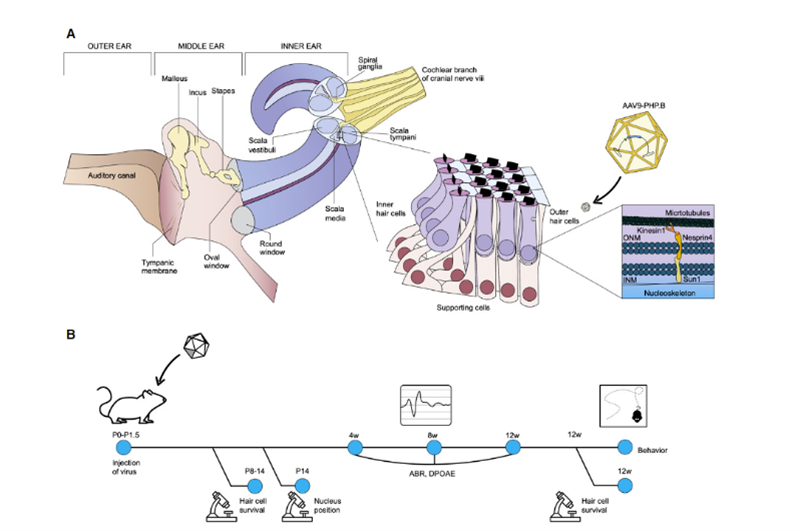
اخیراً، دانشمندان مؤسسه سالک و دانشگاه شفیلد یک نتیجه تحقیقاتی را در درمان مولکولی - روشها و توسعه بالینی [2] منتشر کردند که چشماندازهای کاربردی گستردهای را برای ژندرمانی in vivo ناشنوایی ارثی نشان داد.Uri Manor، استادیار پژوهشی در موسسه Salk و مدیر مرکز Waitt برای بیوفتونیک پیشرفته، گفت که او با کم شنوایی شدید متولد شده است و احساس می کند که بازگرداندن شنوایی یک هدیه فوق العاده خواهد بود.تحقیقات قبلی او نشان داد که Eps8 یک پروتئین تنظیم کننده اکتین با فعالیت های اتصال و درپوش اکتین است.در سلولهای موی حلزون، کمپلکس پروتئینی تشکیلشده توسط Eps8 با MYO15A، WHIRLIN، GPSM2 و GNAI3 عمدتاً بیشتر وجود دارد.بنابراین، Eps8 می تواند طول استریوسیلیای سلول های مو را تنظیم کند، که برای عملکرد طبیعی شنوایی ضروری است.حذف یا جهش Eps8 منجر به استریوسیلیای کوتاه میشود که باعث میشود صدا را به درستی به سیگنالهای الکتریکی برای ادراک مغز تبدیل نکند، که به نوبه خود منجر به ناشنوایی میشود..در همان زمان، والتر مارکوتی، استاد دانشگاه شفیلد، دریافت که سلول های مو در غیاب Eps8 نمی توانند به طور طبیعی رشد کنند.در این مطالعه، Manor و Marcotti با یکدیگر همکاری کردند تا بررسی کنند که آیا افزودن Eps8 به سلولهای stereociliary میتواند عملکرد آنها را بازیابی کند و به نوبه خود، شنوایی را در موش بهبود بخشد.تیم تحقیقاتی از ناقل ویروس مرتبط با آدنو (AAV) Anc80L65 استفاده کرد تا توالی کد کننده حاوی EPS8 نوع وحشی را با تزریق غشای پنجره گرد به حلزون حلزون موش های Eps8-/- P1-P2 تازه متولد شده تحویل دهد.در سلول های موی حلزون موش، عملکرد استریوسیلیا قبل از بلوغ ترمیم شد.و اثر ترمیم با فناوری تصویربرداری و اندازهگیری استریوسیلیا مشخص شد.نتایج نشان داد که Eps8 طول استریوسیلیا را افزایش داد و عملکرد سلول های مو را در سلول های فرکانس پایین ترمیم کرد.آنها همچنین دریافتند که با گذشت زمان، به نظر می رسد سلول ها توانایی خود را برای نجات با این ژن درمانی از دست می دهند.مفهوم این است که این درمان ممکن است نیاز به انجام در داخل رحم داشته باشد، زیرا سلولهای موی Eps8-/- ممکن است بالغ شده باشند یا پس از تولد موشها آسیبی غیرقابل ترمیم انباشته شده باشند.Manor گفت: "Eps8 یک پروتئین با عملکردهای مختلف است و هنوز چیزهای زیادی برای کشف وجود دارد."تحقیقات آینده شامل بررسی تأثیر ژن درمانی Eps8 در بازگرداندن شنوایی در مراحل مختلف رشد، و اینکه آیا ممکن است امکان طولانیتر کردن فرصتهای درمانی وجود داشته باشد، خواهد بود.به طور تصادفی، در نوامبر 2020، پروفسور KarenB Avraham از دانشگاه تل آویو در اسرائیل، نتایج خود را در مجله EMBO Molecular Medicine [3] با استفاده از یک فناوری ژن درمانی نوآورانه برای ایجاد یک ویروس مصنوعی بی ضرر مرتبط با آدنو AAV9-PHP منتشر کرد.ب، نقص ژنی در سلولهای موی موشهای Syne4-/- با تزریق یک ویروس حامل توالی کدکننده Syne4 به گوش داخلی موش ترمیم شد و به آن اجازه داد وارد سلولهای مو شده و مواد ژنتیکی حمل شده را آزاد کند و به آنها اجازه بلوغ و عملکرد طبیعی را میدهد (مانند شکل 2).
شکل 2.نمایش شماتیک آناتومی گوش داخلی، با تمرکز بر اندام کورتی و عملکرد سلولی nesprin-4.
مشاهده می شود که استفاده از ژن درمانی برای دستیابی به هدف درمان بیماری های ارثی در سطح ژن با وارد کردن، حذف یا اصلاح هر گونه ژن جهش یافته برای درمان (یعنی کنترل تغییرات ژنتیکی در بیماری) دارای اثر بالینی بالایی است.چشم انداز برنامهروش های ژن درمانی فعلی برای ناشنوایی با کمبود ژنتیکی را می توان به دسته های زیر تقسیم کرد:
جایگزینی ژن
جایگزینی ژن مسلماً ساده ترین شکل ژن درمانی است که مبتنی بر شناسایی و جایگزینی یک ژن معیوب با یک نسخه طبیعی یا وحشی از ژن است.اولین مطالعه موفق ژن درمانی گوش داخلی برای کاهش شنوایی ناشی از حذف ژن ناقل گلوتامات وزیکولی 3 (VGLUT3).انتقال بیش از حد اگزوژن VGLUT3 با واسطه AAV1 در سلول های مویی گوش داخلی (IHCs) می تواند منجر به بهبود شنوایی پایدار، بهبود مورفولوژی سیناپسی نواری جزئی و پاسخ های تشنجی شود [4].با این حال، در مثالهایی از جمله دو جایگزین ژن تحویلدادهشده با AAV که در مقدمه بالا توضیح داده شد، توجه به این نکته مهم است که مدلهای موشی که برای انواع خاصی از اختلالات کم شنوایی ارثی حذف ژن استفاده میشوند، موقتاً با انسانها متفاوت هستند و در موشهای P1، گوش داخلی در مرحله بلوغ رشد است.در مقابل، انسان ها با گوش داخلی بالغ متولد می شوند.این تفاوت از کاربرد احتمالی نتایج موش برای درمان اختلالات ناشنوایی ارثی انسان جلوگیری می کند مگر اینکه ژن درمانی به گوش موش بالغ داده شود.
ویرایش ژن: CRISPR/Cas9
در مقایسه با «جایگزینی ژن»، توسعه فناوری ویرایش ژن، آغاز درمان بیماری های ژنتیکی را از ریشه به ارمغان آورده است.نکته مهم این است که روش ویرایش ژن کاستیهای روشهای سنتی ژن درمانی با بیان بیش از حد را که برای بیماریهای غالب ناشنوایی ارثی مناسب نیستند، جبران میکند و مشکل این است که روش بیان بیش از حد طولانی مدت طول نمیکشد.پس از اینکه محققان چینی به طور خاص آلل جهش یافته Myo6C442Y را در موش های Myo6WT/C442Y با استفاده از سیستم ویرایش ژن AAV-SaCas9-KKH-Myo6-g2 از بین بردند، و ظرف 5 ماه پس از ناک اوت، موش ها عملکرد شنوایی مدل بازسازی شد.در همان زمان، همچنین مشاهده شد که میزان بقای سلولهای مویی در گوش داخلی بهبود یافته، شکل مژکها منظم شد و شاخصهای الکتروفیزیولوژیک اصلاح شدند [5].این اولین مطالعه در جهان است که از فناوری CRISPR/Cas9 برای درمان ناشنوایی ارثی ناشی از جهش ژن Myo6 استفاده میکند و پیشرفت تحقیقاتی مهم فناوری ویرایش ژن برای درمان ناشنوایی ارثی است.ترجمه بالینی درمان پایه علمی محکمی را فراهم می کند.
روش های انتقال ژن درمانی
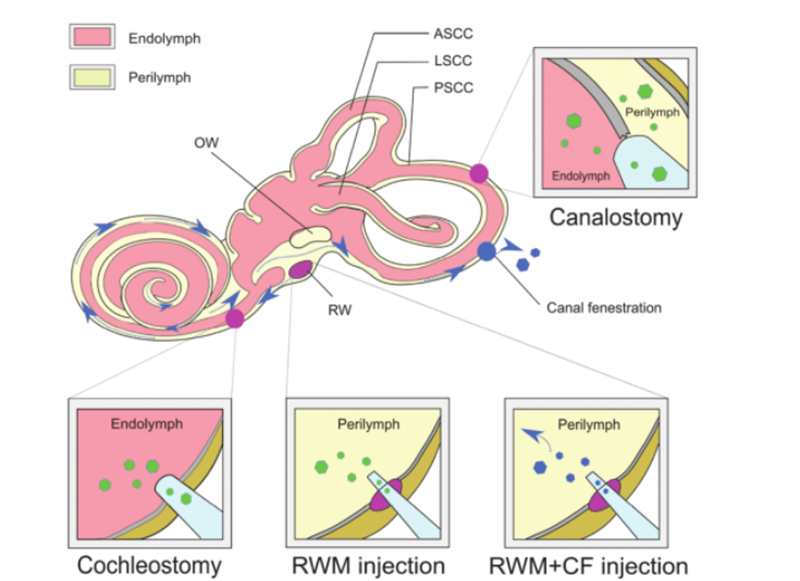
برای موفقیت آمیز بودن ژن درمانی، مولکول های DNA برهنه به دلیل آب دوستی و بار منفی گروه های فسفات نمی توانند به طور موثر به سلول ها نفوذ کنند و برای اطمینان از یکپارچگی مولکول های اسید نوکلئیک مکمل، باید یک روش ایمن و موثر انتخاب شود.DNA تکمیل شده به سلول یا بافت هدف تحویل داده می شود.AAV به دلیل اثر عفونی بالا، ایمنی زایی کم و گرایش وسیع به انواع بافت های مختلف به طور گسترده ای به عنوان یک وسیله انتقال برای درمان بیماری استفاده می شود.در حال حاضر، حجم وسیعی از کار تحقیقاتی جهت گیری زیرگروه های مختلف AAV را نسبت به انواع سلول های مختلف در حلزون موش تعیین کرده است.استفاده از ویژگی های تحویل AAV همراه با پروموترهای اختصاصی سلول می تواند به بیان اختصاصی سلول دست یابد که می تواند اثرات خارج از هدف را کاهش دهد.علاوه بر این، به عنوان جایگزینی برای وکتورهای AAV سنتی، وکتورهای AAV مصنوعی جدید به طور مداوم در حال توسعه هستند و توانایی انتقال برتری را در گوش داخلی نشان میدهند، که AAV2/Anc80L65 بیشترین استفاده را دارد.روشهای تحویل غیر ویروسی را میتوان به روشهای فیزیکی (ریز تزریق و الکتروپوراسیون) و روشهای شیمیایی (پایه لیپیدی، مبتنی بر پلیمر و نانوذرات طلا) تقسیم کرد.هر دو رویکرد در درمان اختلالات ناشنوایی ارثی مورد استفاده قرار گرفتهاند و مزایا و محدودیتهای متفاوتی را نشان دادهاند.علاوه بر وسیله نقلیه تحویل برای ژن درمانی به عنوان یک وسیله، رویکردهای متفاوتی برای تجویز ژن in vivo بر اساس انواع سلول های هدف، مسیرهای تجویز و اثربخشی درمانی می تواند مورد استفاده قرار گیرد.ساختار پیچیده گوش داخلی دسترسی به سلول های هدف را دشوار می کند و توزیع عوامل ویرایش ژنوم کند است.لابیرنت غشایی در لابیرنت استخوانی استخوان تمپورال قرار دارد و شامل مجرای حلزونی، مجرای نیم دایره ای، دهانه رحم و بالون است.جداسازی نسبی آن، حداقل گردش لنفاوی، و جدا شدن از خون توسط یک سد ماز خونی، تحویل سیستمیک مؤثر داروها را فقط به موشهای نوزاد محدود میکند.برای بدست آوردن تیترهای ویروسی مناسب برای ژن درمانی، تزریق موضعی مستقیم ناقل های ویروسی به گوش داخلی ضروری است.راه های تثبیت شده تزریق عبارتند از: (1) غشای پنجره گرد (RWM)، (2) تراکئوستومی، (3) کوکلئوستومی اندولنفاتیک یا پری لنفاتیک، (4) غشای پنجره گرد به علاوه فنستراسیون لوله (CF) (مانند شکل 3).
شکل 3.انتقال ژن درمانی به گوش داخلی
اگرچه پیشرفت های زیادی در زمینه ژن درمانی انجام شده است، اما بر اساس اهداف ترجمه بالینی، باید کارهای بیشتری انجام شود تا ژن درمانی بتواند به گزینه درمانی خط اول برای بیماران مبتلا به بیماری های ژنتیکی تبدیل شود، به ویژه در توسعه ناقل های ایمن و موثر و روش تحویل.اما ما بر این باوریم که در آینده نزدیک، این نوع درمان ها به یکی از اصلی ترین درمان های شخصی تبدیل خواهند شد و تأثیر بسیار مثبتی بر زندگی افراد مبتلا به اختلالات ژنتیکی و خانواده های آنها خواهند داشت.
Foregene همچنین یک کیت غربالگری با کارایی بالا برای ژن های هدف راه اندازی کرده است که سریع است و می تواند رونویسی معکوس و واکنش های qPCR را بدون استخراج RNA انجام دهد.
لینک های محصول
کیت Cell Direct RT-qPCR — Taqman/SYBR GREEN I
برای اطلاعات بیشتر محصول لطفا تماس بگیرید:
زمان ارسال: سپتامبر-02-2022