در کنفرانس واکسن و سلامت، کارشناسان خواستار این شدند که «همه باید به واکسنهای mRNA توجه کنند که تفکر نامحدودی را برای انسان فراهم میکند».بنابراین واکسن mRNA دقیقا چیست؟چگونه کشف شد و ارزش کاربردی آن چقدر است؟آیا می تواند در برابر COVID-19 که در سراسر جهان موج می زند مقاومت کند؟آیا کشور من واکسن mRNA را با موفقیت تولید کرده است؟امروز، بیایید با گذشته و حال واکسنهای mRNA آشنا شویم.
01
mRNA در واکسن های mRNA چیست؟
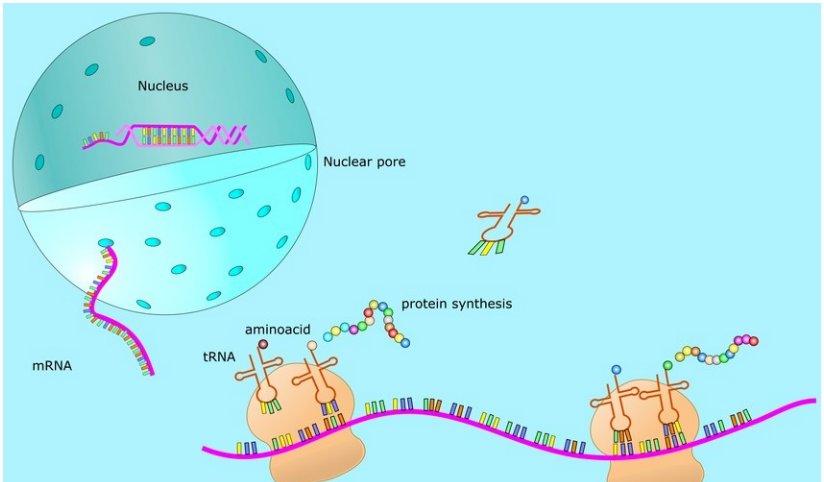
mRNA (مسنجر RNA)، یعنی RNA پیام رسان، نوعی RNA تک رشته ای است که از یک رشته DNA به عنوان یک الگو رونویسی می شود و حامل اطلاعات ژنتیکی است که می تواند سنتز پروتئین را هدایت کند.به زبان ساده، mRNA اطلاعات ژنتیکی یک رشته DNA دو رشتهای را در هسته تکرار میکند و سپس از هسته خارج میشود تا پروتئینهایی در سیتوپلاسم تولید کند.در سیتوپلاسم، ریبوزوم ها در امتداد mRNA حرکت می کنند، توالی پایه آن را می خوانند و آن را به اسید آمینه مربوطه خود ترجمه می کنند و در نهایت پروتئینی را تشکیل می دهند (شکل 1).
شکل 1 فرآیند کار mRNA
02
واکسن mRNA چیست و چه چیزی آن را منحصر به فرد می کند؟
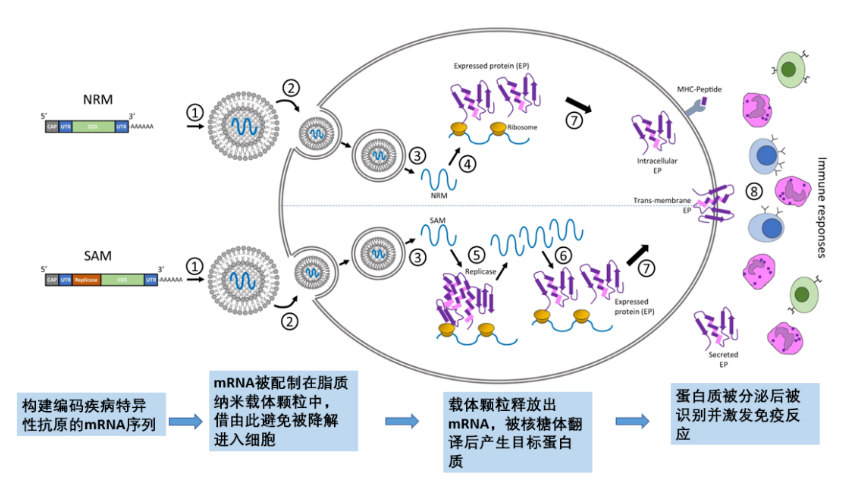
واکسنهای mRNA، mRNA کدکننده آنتیژنهای خاص بیماری را به بدن وارد میکنند و از مکانیسم سنتز پروتئین سلول میزبان برای تولید آنتیژن استفاده میکنند و در نتیجه پاسخ ایمنی را تحریک میکنند.معمولاً، توالیهای mRNA از آنتیژنهای خاص را میتوان بر اساس بیماریهای مختلف ساخت، بستهبندی و توسط ذرات نانوحامل لیپیدی جدید به سلولها منتقل شد و سپس توالیهای mRNA ریبوزومهای انسانی برای ترجمه توالیهای mRNA برای تولید پروتئینهای آنتیژن بیماری، که توسط سیستم خودایمنی به عنوان یک نقش ایمنی پس از ترشح شناخته میشوند، استفاده میشوند.
بنابراین، چه چیزی در مورد این نوع واکسن mRNA در مقایسه با واکسن های سنتی منحصر به فرد است؟واکسنهای mRNA پیشرفتهترین واکسنهای نسل سوم هستند و تحقیقات بیشتری برای افزایش پایداری، تنظیم ایمنیزایی آنها و توسعه فناوریهای تحویل جدید مورد نیاز است.
نسل اول واکسنهای سنتی عمدتاً شامل واکسنهای غیرفعال و واکسنهای تضعیف شده زنده هستند که بیشترین استفاده را دارند.واکسنهای غیرفعال ابتدا به کشت ویروسها یا باکتریها و سپس غیرفعال کردن آنها با گرما یا مواد شیمیایی (معمولاً فرمالین) اشاره دارند.واکسنهای زنده ضعیف شده به پاتوژنهایی اطلاق میشوند که پس از درمانهای مختلف جهش مییابند و سمیت آنها را ضعیف میکنند.اما همچنان ایمنی زایی خود را حفظ کرده است.تلقیح آن به بدن باعث بروز بیماری نمی شود، اما عامل بیماری زا می تواند در بدن رشد کرده و تکثیر شود، پاسخ ایمنی بدن را تحریک کند و در به دست آوردن محافظت طولانی مدت یا مادام العمر نقش داشته باشد.
نسل دوم واکسنهای جدید شامل واکسنهای زیر واحد و واکسنهای پروتئین نوترکیب است.واکسن زیرواحد یک واکسن زیرواحد واکسنی است که از اجزای اصلی ایمونوژن محافظ باکتری های بیماری زا ساخته شده است، یعنی از طریق تجزیه شیمیایی یا پروتئولیز کنترل شده، ساختار پروتئینی ویژه باکتری ها و ویروس ها استخراج و غربال می شود.واکسن های ساخته شده از قطعات فعال ایمونولوژیک؛واکسن های پروتئین نوترکیب، پروتئین های نوترکیب آنتی ژنی هستند که در سیستم های بیان سلولی مختلف تولید می شوند.
نسل سوم واکسن های پیشرفته شامل واکسن های DNA و واکسن های mRNA است.وارد کردن مستقیم قطعه ژن ویروسی (DNA یا RNA) کدکننده پروتئین آنتی ژنی خاص به سلول های بدنی حیوانی (تزریق واکسن به بدن انسان) و تولید پروتئین آنتی ژنی از طریق سیستم سنتز پروتئین سلول میزبان، و القای میزبان برای ایجاد ایمنی در برابر پاسخ پروتئین آنتی ژنی به منظور دستیابی به هدف پیشگیری و درمان بیماری است.تفاوت بین این دو در این است که DNA ابتدا به mRNA رونویسی می شود و سپس پروتئین سنتز می شود، در حالی که mRNA مستقیماً سنتز می شود.
03
تاریخچه کشف و ارزش کاربرد واکسن mRNA
وقتی صحبت از واکسنهای mRNA به میان میآید، باید به یک دانشمند زن برجسته به نام کتی کاریکو اشاره کنیم که پایه و اساس تحقیقات علمی محکمی برای ظهور واکسنهای mRNA گذاشته است.او در حین تحصیل علاقه زیادی به mRNA داشت.او در بیش از 40 سال فعالیت علمی پژوهشی خود دچار شکست های مکرر شد، درخواستی برای بودجه تحقیقات علمی نکرد و جایگاه پژوهشی علمی ثابتی نداشت، اما همیشه بر تحقیقات mRNA تاکید داشته است.
سه گره مهم در ظهور واکسنهای mRNA وجود دارد.
در اولین قدم، او موفق شد مولکول mRNA مورد نظر را از طریق کشت سلولی تولید کند، اما در ساختن عملکرد mRNA در بدن با مشکل مواجه شد: پس از تزریق mRNA به موش، توسط سیستم ایمنی بدن موش بلعیده میشود.سپس با ویسمن آشنا شد.آنها از مولکولی در tRNA به نام پسودوریدین برای فرار mRNA از پاسخ ایمنی استفاده کردند.[2].
در مرحله دوم، در حدود سال 2000، پروفسور پیتر کولیس LNPهای نانوتکنولوژی لیپیدی را برای تحویل in vivo siRNA برای کاربردهای خاموش کردن ژن مورد مطالعه قرار داد [3][4].سازمان وایزمن Kariko و همکاران.دریافتند که LNP حامل مناسب mRNA در داخل بدن است و ممکن است به ابزاری ارزشمند برای ارائه پروتئینهای درمانی کدکننده mRNA تبدیل شود و متعاقباً در پیشگیری از ویروس زیکا، HIV و تومورها تأیید شود [5] [6] [7] [8].
در مرحله سوم، در سال های 2010 و 2013، Moderna و BioNTech به طور متوالی مجوزهای ثبت اختراع مربوط به سنتز mRNA را از دانشگاه پنسیلوانیا برای توسعه بیشتر دریافت کردند.کاتالین همچنین در سال 2013 معاون ارشد BioNTech برای توسعه بیشتر واکسنهای mRNA شد.
امروزه از واکسنهای mRNA میتوان در بیماریهای عفونی، تومورها و آسم استفاده کرد.در مورد کووید-19 که در سراسر جهان موج می زند، واکسن های mRNA ممکن است نقش پیشتاز را ایفا کنند.
04
چشم انداز کاربرد واکسن mRNA در COVID-19
با اپیدمی جهانی کووید-19، کشورها سخت تلاش می کنند تا واکسنی برای مهار این همه گیری ایجاد کنند.به عنوان یک نوع جدید واکسن، واکسن mRNA نقش مهمی در ظهور اپیدمی جدید تاج دارد.بسیاری از مجلات برتر نقش mRNA را در ویروس کرونا جدید SARS-CoV-2 گزارش کرده اند (شکل 3).
شکل 3 گزارش واکسنهای mRNA برای جلوگیری از کروناویروس جدید (از NCBI)
اول از همه، بسیاری از دانشمندان تحقیقات واکسن mRNA (SARS-CoV-2 mRNA) را علیه کروناویروس جدید در موش ها گزارش کرده اند.به عنوان مثال: واکسن mRNA (mRNA-LNP) اصلاح شده با نانوذرات لیپیدی، یک تزریق تک دوز، پاسخ سلول های CD4+ T و CD8+ T نوع 1 قوی، پاسخ سلول های B پلاسما و حافظه طولانی مدت، و پاسخ آنتی بادی خنثی کننده قوی و پایدار را القا می کند.این نشان میدهد که واکسن mRNA-LNP یک کاندید امیدوارکننده در برابر COVID-19 است[9][10].
دوم، برخی از دانشمندان اثرات mRNA SARS-CoV-2 و واکسن های سنتی را با هم مقایسه کردند.در مقایسه با واکسنهای پروتئین نوترکیب: واکسنهای mRNA در پاسخ به مرکز ژرمینال، فعالسازی Tfh، تولید آنتیبادی خنثیکننده، سلولهای B حافظه خاص و سلولهای پلاسما با عمر طولانی بسیار برتر از واکسنهای پروتئینی هستند [11].
سپس، زمانی که نامزدهای واکسن mRNA SARS-CoV-2 وارد آزمایشهای بالینی شدند، نگرانیهایی در مورد کوتاه مدت حفاظت از واکسن ایجاد شد.دانشمندان شکل محصور شده با چربی از واکسن mRNA اصلاح شده با نوکلئوزید به نام mRNA-RBD را ساخته اند.یک تزریق میتواند آنتیبادیهای خنثیکننده قوی و پاسخهای سلولی ایجاد کند و تقریباً میتواند از موشهای مدل آلوده به 2019-nCoV محافظت کند و سطوح بالایی از آنتیبادیهای خنثیکننده حداقل به مدت 6.5 ماه حفظ شود.این داده ها نشان می دهد که یک دوز واحد mRNA-RBD محافظت طولانی مدت در برابر چالش SARS-CoV-2 را فراهم می کند [12].
همچنین دانشمندانی در حال کار برای تولید واکسنهای ایمن و مؤثر جدید علیه کووید-19، مانند واکسن BNT162b هستند.ماکاکوهای محافظت شده از SARS-CoV-2، از دستگاه تنفسی تحتانی در برابر RNA ویروسی محافظت کردند، آنتی بادی های بسیار قوی تولید کردند و هیچ نشانه ای از افزایش بیماری نشان ندادند.دو نامزد در حال حاضر در مرحله آزمایشی مرحله I تحت ارزیابی هستند، و ارزیابی در آزمایشات جهانی مرحله II/III نیز در حال انجام است، و درخواست در حال حاضر در گوشه و کنار است [13].
05
وضعیت واکسن mRNA در جهان
در حال حاضر، BioNTech، Moderna و CureVac به عنوان سه رهبر برتر درمان mRNA در جهان شناخته می شوند.در میان آنها، BioNTech و Moderna در خط مقدم تحقیق و توسعه واکسن جدید تاج هستند.مدرنا بر تحقیق و توسعه داروها و واکسن های مرتبط با mRNA تمرکز کرده است.واکسن آزمایشی فاز سوم کووید-19 mRNA-1273 سریعترین پروژه در حال رشد این شرکت است.BioNTech همچنین یک شرکت تحقیق و توسعه دارو و واکسن mRNA در جهان است که در مجموع 19 دارو/واکسن mRNA دارد که 7 مورد از آنها وارد مرحله بالینی شده اند.CureVac بر تحقیق و توسعه داروها/واکسنهای mRNA تمرکز کرده است و اولین شرکتی در جهان است که خط تولید RNA منطبق با GMP را با تمرکز بر تومورها، بیماریهای عفونی و بیماریهای نادر ایجاد میکند.
محصولات مرتبط:مهارکننده RNase
کلمات کلیدی: واکسن miRNA، جداسازی RNA، استخراج RNA، مهارکننده RNase
مراجع: 1.K Karikó، Buckstein M، Ni H، و همکاران.سرکوب تشخیص RNA توسط گیرنده های Toll مانند: تأثیر اصلاح نوکلئوزیدی و منشاء تکاملی RNA [J].مصونیت، 2005، 23 (2): 165-175.
2. K Karikó، Muramatsu H، ولز FA، و همکاران.الحاق سودوریدین به mRNA ناقل غیر ایمنی زا برتر را با افزایش ظرفیت انتقالی و پایداری بیولوژیکی ایجاد می کند [J].درمان مولکولی، 2008.3.Chonn A، Cullis PR.پیشرفتهای اخیر در فنآوریهای لیپوزوم و کاربردهای آنها برای تحویل ژن سیستمیک [J].بررسی های پیشرفته تحویل دارو، 1998، 30 (1-3): 73.4.Kulkarni JA، Witzigmann D، Chen S، و همکاران.فناوری نانوذرات لیپیدی برای ترجمه بالینی siRNA درمانی [J].حساب های تحقیقات شیمیایی، 2019، 52 (9).5.کاریکو، کاتالین، مدن و همکاران.سینتیک بیان mRNA ژن اصلاح شده با نوکلئوزید که در نانوذرات لیپیدی از مسیرهای مختلف به موش تحویل داده می شود [J].مجله انتشار کنترل شده مجله رسمی انجمن انتشار کنترل شده، 2015.6.محافظت از ویروس زیکا با یک واکسیناسیون mRNA اصلاح شده با نوکلئوزید با دوز پایین [J].طبیعت، 2017، 543(7644):248-251.7.Pardi N، Secreto AJ، Shan X، و همکاران.تجویز mRNA اصلاح شده با نوکلئوزید که آنتی بادی خنثی کننده گسترده را کد می کند، از موش های انسانی شده در برابر چالش HIV-1 [J] محافظت می کند.Nature Communications, 2017, 8:14630.8.Stadler CR، B?Hr-Mahmud H، Celik L، و همکاران.از بین بردن تومورهای بزرگ در موش توسط آنتی بادی های دوویژه کدگذاری شده با mRNA [J].طب طبیعت، 2017.9.NN Zhang، Li XF، Deng YQ، و همکاران.یک واکسن mRNA مقاوم در برابر حرارت در برابر COVID-19[J].سلول، 10.2020.D Laczkó، Hogan MJ، Toulmin SA، و همکاران.یک ایمنسازی منفرد با واکسنهای mRNA اصلاحشده با نوکلئوزید، پاسخهای ایمنی سلولی و هومورال قوی علیه SARS-CoV-2 در موشها ایجاد میکند - ScienceDirect[J].2020.11.Lederer K، Castao D، Atria DG، و همکاران.واکسنهای mRNA SARS-CoV-2 پاسخهای مرکز ژرمینال اختصاصی آنتیژن قوی مرتبط با تولید آنتیبادی خنثیکننده [J] را تقویت میکنند.مصونیت، 2020، 53(6):1281-1295.e5.12.هوانگ کیو، جی کی، تیان اس، و همکاران.یک واکسن تک دوز mRNA یک محافظت طولانی مدت برای موش های تراریخته hACE2 از SARS-CoV-2[J] فراهم می کند.Nature Communications.13.Vogel AB، Kanevsky I، Ye C، و همکاران.واکسنهای ایمونوژنیک BNT162b از ماکاکهای رزوس در برابر SARS-CoV-2[J] محافظت میکنند.طبیعت، 2021: 1-10.
زمان ارسال: ژوئن-20-2022