واکسن mRNA چیست؟
واکسن mRNA، RNA را به سلولهای بدن منتقل میکند تا پس از اصلاحات مربوطه در شرایط آزمایشگاهی، آنتیژنهای پروتئینی را بیان و تولید کند، در نتیجه بدن را به تولید پاسخ ایمنی در برابر آنتیژن هدایت میکند و در نتیجه ظرفیت ایمنی بدن را افزایش میدهد.[1,3].
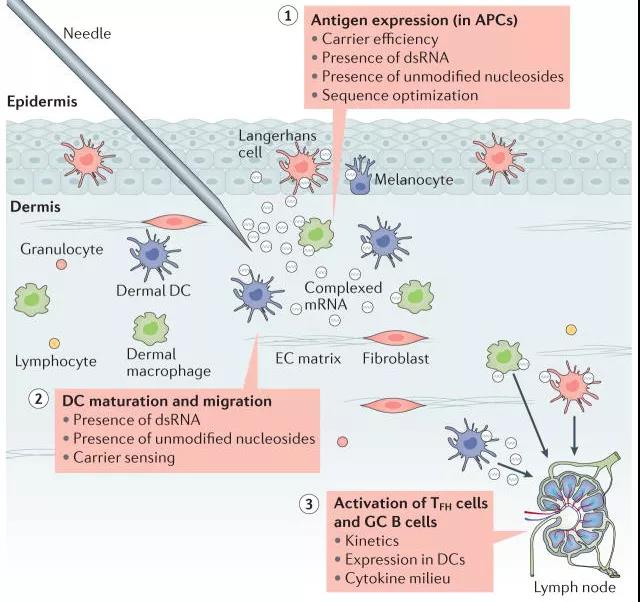
شکل 1: نمودار شماتیک اثر تزریق مستقیم واکسن mRNA [2]
طبقه بندی واکسن های mRNA
واکسنهای mRNA به دو نوع تقسیم میشوند:غیر تکراریmRNA وخود تقویت کنندهmRNA: mRNA خودتقویت شونده نه تنها آنتی ژن هدف را رمزگذاری می کند، بلکه همانندسازی را نیز رمزگذاری می کند که تکثیر RNA داخل سلولی و مکانیسم بیان پروتئین را امکان پذیر می کند.واکسنهای mRNA غیر تکثیر شونده فقط آنتیژنهای هدف را رمزگذاری میکنند و دارای مناطق ترجمهنشده ۵ و ۳ (UTR) هستند.آنها تحریک جامع سازگاری و ایمنی ذاتی، یعنی بیان آنتی ژن درجا و انتقال سیگنال خطر را فراهم می کنند و دارای ویژگی های کاربردی زیر هستند.[2،3]
● می تواند تحریک جامع سازگاری و ایمنی ذاتی، یعنی بیان آنتی ژن درجا و انتقال سیگنال خطر را فراهم کند.
● می تواند یک پاسخ ایمنی "متعادل"، از جمله عوامل هومورال و سلولی و حافظه ایمنی را القا کند.
● می تواند آنتی ژن های مختلف را بدون افزایش پیچیدگی فرمول واکسن ترکیب کند
● بهبود مستمر پتانسیل ایمنی را می توان از طریق واکسیناسیون مکرر به دست آورد، و پاسخ ایمنی به ناقل وجود ندارد یا کم است.
واکسن های mRNA پایدار در برابر حرارت می توانند حمل و نقل و ذخیره سازی واکسن ها را ساده کنند
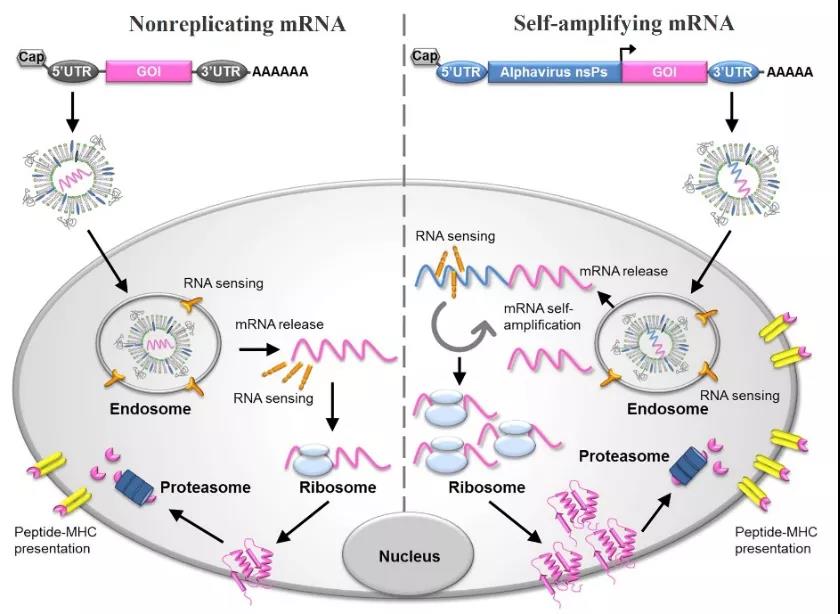
شکل 2: نمودار شماتیک واکسن mRNA و مکانیسم بیان آنتی ژن آن [4]
ویژگی های واکسن های mRNA
در مقایسه با واکسنهای سنتی، واکسنهای mRNA فرآیند تولید ساده، سرعت توسعه سریع، عدم نیاز به کشت سلولی و هزینه کم دارند.در مقایسه با واکسنهای DNA، واکسنهای mRNA نیازی به ورود به هسته ندارند و خطر ادغام در ژنوم میزبان وجود ندارد.نیمه عمر را می توان با اصلاح تنظیم کرد.
جدول 1: مزایا و معایب واکسن های mRNA
|
| مزیت - فایده - سود - منفعت | کمبود |
| واکسن mRNA | تحقیق و توسعه سریع، تولید واکسن تنها 40 روز طول می کشد | یک پاسخ ایمنی غیر ضروری را تحریک کنید
|
| بی ثباتی mRNA در شرایط فیزیولوژیکی، به راحتی تجزیه می شود | برای جلوگیری از جهش های درمانی احتمالی در ژنوم ادغام نمی شود
| |
| بدون نیاز به هیچ سیگنال محلی سازی هسته ای، رونویسی | اثربخشی ایمنی هسته ای هنوز باید تأیید شود
|
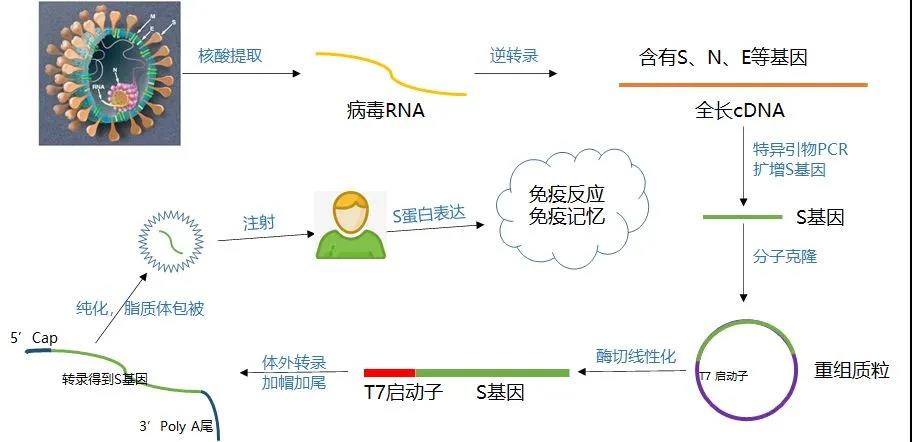
شکل 3: نمودار جریان تولید و تهیه واکسن mRNA [4]
کیت جداسازی RNA ویروسی Foregene
RT-qPCR آسان (یک مرحله ای)
استراتژیهای بهبود یافته برای تهیه واکسنهای mRNA
به دلیل پایداری ضعیف خود mRNA، تجزیه آسان توسط نوکلئازها در بافت ها، راندمان پایین ورود به سلول و بازده ترجمه پایین، این نقص ها کاربرد واکسن های mRNA را محدود می کند.کارایی ترجمه نیز نقش بسیار مهمی دارد.وسایل نقلیه تحویل را می توان به ناقل های ویروسی و ناقل های غیر ویروسی (شامل لیپوزوم ها، غیر لیپوزوم ها، ویروس ها، نانوذرات و غیره) تقسیم کرد.بنابراین، اقدامات بهبود مربوطه مورد نیاز است.در زیر یک استراتژی بهبود فارماکولوژیک برای تهیه mRNA ارائه شده است[2]
1 آنالوگ های کلاهک را سنتز کنید یا از آنزیم های پوشاننده برای تثبیت mRNA و افزایش ترجمه پروتئین با اتصال به فاکتور شروع ترجمه یوکاریوتی 4E (EIF4E) استفاده کنید.
2 عناصر موجود در ناحیه ترجمه نشده 5' (UTR) و 3'-UTR را برای تثبیت mRNA و افزایش ترجمه پروتئین تنظیم کنید.
3 افزودن دم Poly(A) می تواند mRNA را تثبیت کند و ترجمه پروتئین را افزایش دهد
4 نوکلئوزیدهای اصلاح شده برای کاهش فعال سازی ذاتی ایمنی و افزایش ترجمه
5 درمان با RNase III و خالص سازی کروماتوگرافی مایع پروتئین سریع (FPLC) می تواند فعال سازی ایمنی را کاهش داده و ترجمه را افزایش دهد.
6 دنباله ها یا کدون ها را برای افزایش ترجمه بهینه کنید
7 ارائه همزمان فاکتورهای شروع ترجمه و سایر روش ها برای تغییر ترجمه و ایمنی زایی
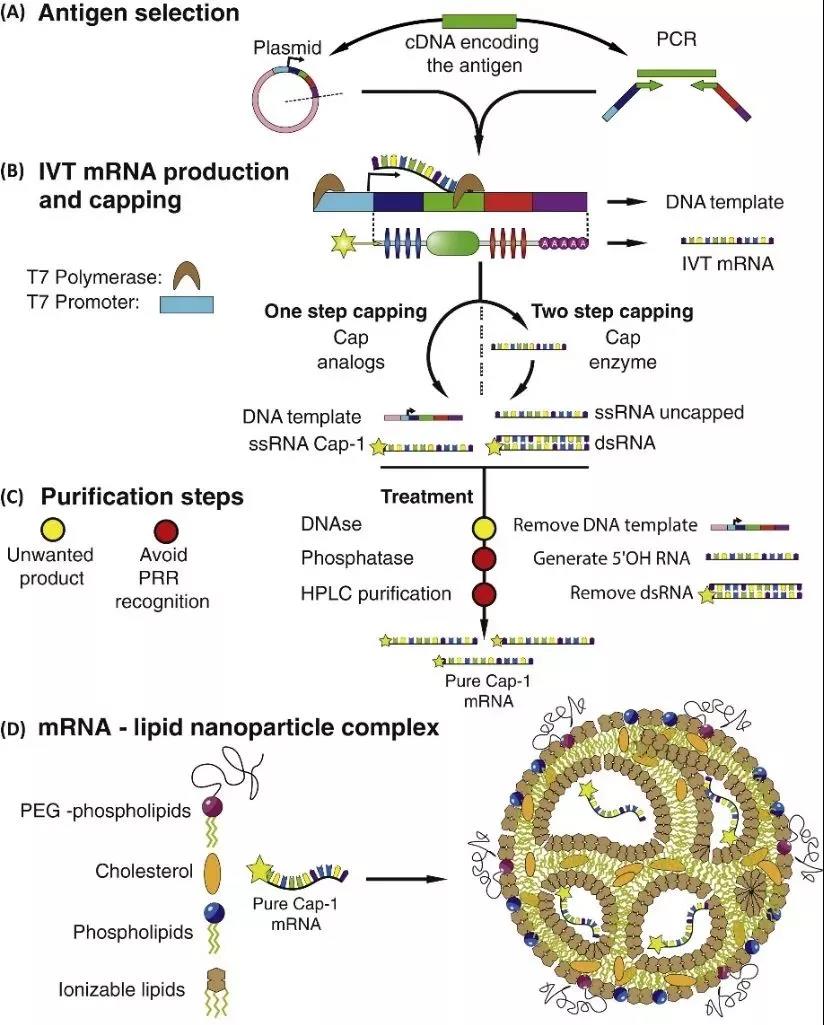
شکل 4: فرآیند تولید و مونتاژ mRNA رونویسی in vitro (IVT) [5]
تهیه DNA پلاسمید در مقیاس بزرگ
خالص سازی DNA پلاسمید عمدتاً آلاینده هایی مانند RNA، اندوتوکسین DNA دایره باز، پروتئین میزبان و اسید نوکلئیک میزبان را حذف می کند و معمولاً پلاسمید نوترکیب را به E. coli تبدیل می کند.E. coli تحت تخمیر با چگالی بالا، سپس جداسازی جامد از مایع و جمع آوری E. coli قرار می گیرد.E. coli سپس تحت لیز قلیایی، جداسازی جامد-مایع گریز از مرکز و شفاف سازی میکروفیلتراسیون پس از لیز، اولترافیلتراسیون و غلظت پس از شفاف سازی، و سپس خالص سازی کروماتوگرافی قرار می گیرد.

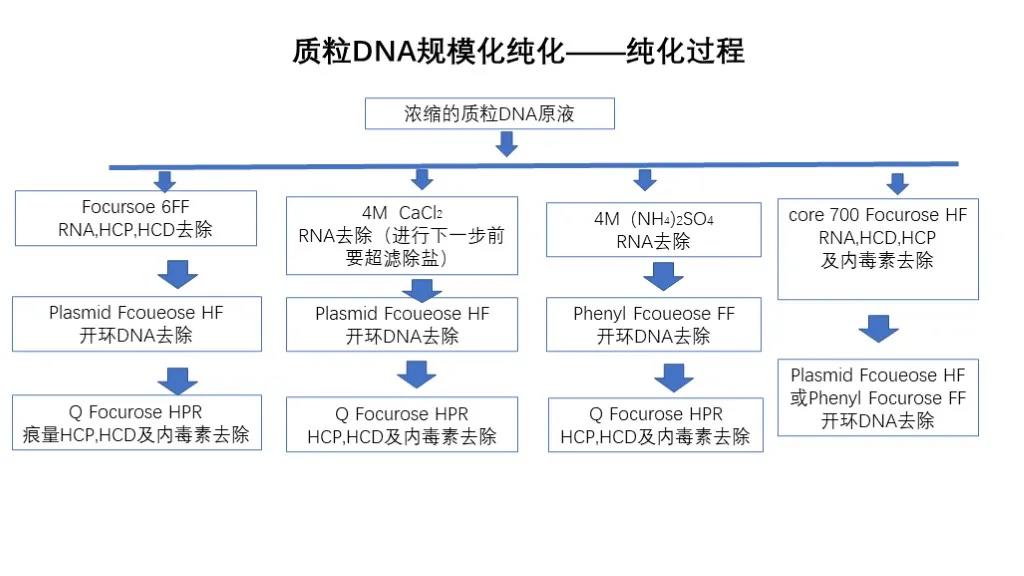
خالص سازی DNA پلاسمید:
کیت مینی پلاسمید جنرال Foregene
【1】苗鹤凡, 郭勇, 江新香.mRNA疫苗研究进展及挑战[ج].免疫学杂志، 2016 (05): 446-449.
【2】پردی ان، هوگان ام جی، پورتر اف دبلیو، و همکاران.واکسنهای mRNA - عصر جدیدی در واکسنشناسی [J].Nature Reviews Drug Discovery، 2018.
【3】Kramps T., Elbers K. (2017) مقدمه ای بر واکسن های RNA.در: Kramps T.، Elbers K. (eds) RNA Vaccines.Methods in Molecular Biology, vol 1499. Humana Press, New York, NY.
【4】Maruggi G، Zhang C، Li J، و همکاران.mRNA به عنوان یک فناوری تبدیلکننده برای توسعه واکسن برای کنترل بیماریهای عفونی [J].درمان مولکولی، 2019.
【5】سرجیو لینارس-فرناندز، سلین لاکروآ، تنظیم واکسن mRNA برای متعادل کردن پاسخ ایمنی ذاتی/تطبیقی، روندها در پزشکی مولکولی، جلد 26، شماره 3،2020، صفحات 311-323.
زمان ارسال: اوت-05-2021








